Наследствен неполипозен колоректален рак (HNPCC), също наричан Синдром на Линч, е автозомно доминиращо генетично състояние, което е свързано с висок риск от рак на дебелото черво, както и други видове рак, включително рак на ендометриума (втори по честота), яйчници, стомах, тънки черва, хепатобилиарни пътища, горни пикочни пътища, мозък и кожа. Повишеният риск за тези видове рак се дължи на наследени мутации, които влошават възстановяването на несъответствието на ДНК. Това е вид синдром на рака.
Симптоми на синдрома на Линч
Риск от рак
Доживотен риск и средна възраст при диагностициране на рак, свързан със синдрома на Lynch
| Вид рак | Доживотен риск (%) | Средна възраст при поставяне на диагнозата (години) |
| Колоректален | 52-58 | 44-61 |
| Ендометриална | 25-60 | 48-62 |
| Стомашни | 6-13 | 56 |
| Яйчници | 4-12 | 42.5 |
В допълнение към видовете рак, открити в диаграмата по-горе, се разбира, че синдромът на Lynch също допринася за повишен риск от рак на тънките черва, рак на панкреаса, рак на уретера / бъбречното легенче, рак на жлъчните пътища, мозъчен рак и мастни новообразувания. Повишеният риск от рак на простатата и рак на гърдата също е свързан със синдрома на Линч, въпреки че тази връзка не е напълно разбрана.
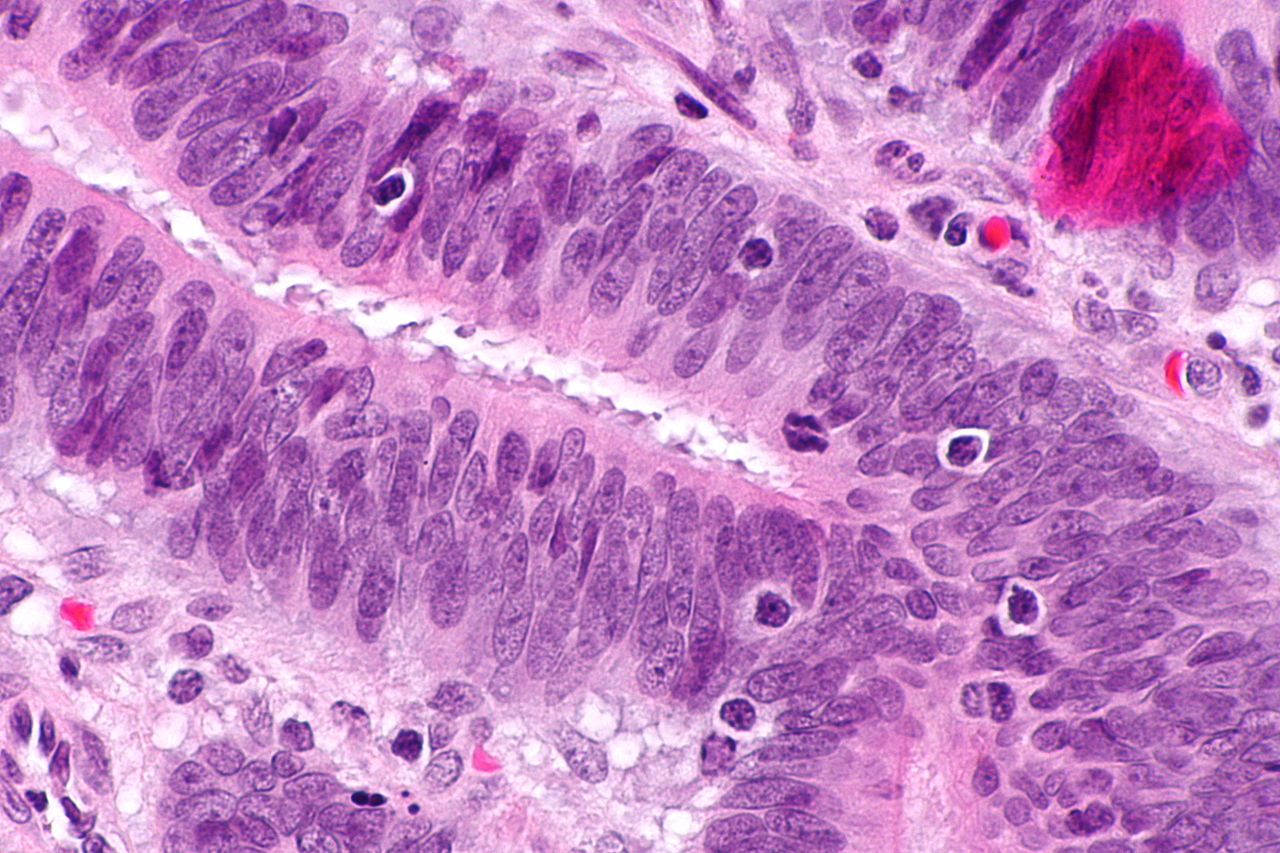
Две трети от рак на дебелото черво се появяват в проксималното дебело черво, а често срещаните признаци и симптоми включват кръв в изпражненията, диария или запек и неволна загуба на тегло. Средната възраст на диагнозата колоректален рак е 44 за членове на семейства, които отговарят на критериите от Амстердам. Средната възраст на диагностициране на рак на ендометриума е около 46 години. Сред жените с HNPCC, които имат както рак на дебелото черво, така и на ендометриума, около половината от тях се срещат първо с рак на ендометриума, което прави рак на ендометриума най-честият рак на сентинела при синдрома на Lynch. Най-честият симптом на рак на ендометриума е необичайно вагинално кървене. При HNPCC средната възраст на диагностициране на рак на стомаха е 56-годишна възраст, като аденокарциномът от чревен тип е най-често съобщаваната патология. Свързаният с HNPCC рак на яйчниците има средна диагноза на възраст 42,5 години; приблизително 30% са диагностицирани преди 40-годишна възраст.
Установена е значителна вариация в честотата на рака в зависимост от съответната мутация. До 75-годишна възраст рисковете от колоректален рак, рак на ендометриума, рак на яйчниците, горната част на стомашно-чревния тракт (стомаха, дванадесетопръстника, жлъчния канал или панкреаса), рак на пикочните пътища, рак на простатата и мозъчни тумори са както следва: за мутации на MLH1 рискът е съответно 46%, 43%, 10%, 21%, 8%, 17% и 1%; за мутации на MSH2 рисковете бяха съответно 57%, 17%, 10%, 25%, 32% и 5%; за мутации на MSH6 рисковете бяха съответно 15%, 46%, 13%, 7%, 11%, 18% и 1%.
| Ген | Риск от рак на яйчниците | Риск от рак на ендометриума |
|---|---|---|
| MLH1 | 4-24% | 25-60% |
| MSH2 / EPCAM | 4-24% | 25-60% |
| MSH6 | 1-11% | 16-26% |
| PMS2 | 6% (комбиниран риск) | 15% |
Генетика

HNPCC се наследява по автозомно доминиращ начин. Отличителният белег на HNPCC е дефектно възстановяване на несъответствието на ДНК, което причинява повишена скорост на единични нуклеотидни промени и микросателитна нестабилност, известна още като MSI-H (H е „висока“). MSI може да се идентифицира в проби от рак в патологичната лаборатория. Повечето случаи водят до промени в дължините на динуклеотидни повторения на нуклеобазите цитозин и аденин (последователност: CACACACACA …).
Четирите основни гена, участващи в HNPCC, обикновено кодират протеини, които образуват димери, за да функционират:
- MLH1 протеинът се димеризира с PMS2 протеин, за да образува MutLα, който координира свързването на други протеини, участващи в възстановяването на несъответствие като ДНК хеликаза, едноверижен ДНК свързващ протеин (RPA) и ДНК полимерази.
- Протеинът MSH2 се димеризира с протеин MSH6, който идентифицира несъответствия чрез модел на плъзгаща скоба, протеин за сканиране за грешки.
Нарушаването на двата гена за протеиновия димер нарушава протеиновата функция. Тези 4 гена участват в корекция на грешки (поправка на несъответствие), така че дисфункцията на гените може да доведе до невъзможност да се поправят грешки в репликацията на ДНК и да причини HNPCC. Известно е, че HNPCC е свързан с други мутации в гени, участващи в пътя на възстановяване на несъответствието на ДНК:
| Име на OMIM | Гени, замесени в HNPCC | Честота на мутации в семейства HNPCC | Локус | Първа публикация |
|---|---|---|---|---|
| HNPCC1 (120435) | MSH2 / EPCAM | приблизително 60% | 2р22 | Фишел 1993г |
| HNPCC2 (609310) | MLH1 | приблизително 30% | 3р21 | Пападопулос 1994 |
| HNPCC5 | MSH6 | 7-10% | 2р16 | Мияки 1997 |
| HNPCC4 | PMS2 | относително рядко | 7p22 | Николаидес 1994 |
| HNPCC3 | PMS1 | доклад за случая | 2q31-q33 | Николаидес 1994 |
| HNPCC6 | TGFBR2 | доклад за случая | 3р22 | |
| HNPCC7 | MLH3 | оспорен | 14q24.3 |
Повечето хора с HNPCC наследяват състоянието от родител. Въпреки това, поради непълна проникване, променлива възраст на диагнозата рак, намаляване на риска от рак или ранна смърт, не всички хора с мутация на ген HNPCC имат родител, който е имал рак. Някои хора развиват HNPCC de-novo в ново поколение, без да наследяват гена. Тези хора често се идентифицират само след развитие на ранен рак на дебелото черво. Родителите с HNPCC имат 50% шанс да предадат генетичната мутация на всяко дете. Също така е важно да се отбележи, че вредната мутация само на един от MMR гените не е достатъчна, за да причини рак, но че по-скоро трябва да се появят по-нататъшни мутации в други гени на супресор на тумора.
Диагностика на синдрома на Линч
Диагноза на синдрома на Lynch се прилага при хора с ДНК мутация на зародишна линия в един от MMR гените (MLH1, MSH2, MSH6 и PMS2) или гена EPCAM, идентифициран чрез генетично тестване. Кандидатите за генетично тестване на зародишни линии могат да бъдат идентифицирани по клинични критерии като Амстердамските клинични критерии и насоки на Bethesda, или чрез туморен анализ чрез имунохистохимия (IHC) или тестване на микросателитна нестабилност (MSI). В САЩ професионалните общества препоръчват да се тества всеки рак на дебелото черво за MSI или IHC като скрининг за синдром на Lynch, но това не винаги се извършва поради ограничения на разходите и ресурсите. Генетичното изследване се предлага на пазара и се състои от кръвен тест.
Имунохистохимия
Имунохистохимията (IHC) е метод, който може да се използва за откриване на експресия на анормално несъответствие (MMR) при тумори, които са свързани със синдрома на Lynch. Въпреки че не е диагностично за синдром на Lynch, той може да играе роля при идентифицирането на хора, които трябва да имат тестване на зародишна линия. Два метода за прилагане на IHC тестване включват възрастово тестване и универсално тестване за всички хора. Понастоящем няма широко съгласие относно това кой метод на скрининг да се използва. Въз основа на възрастта тестове за IHC се предлагат отчасти поради анализи на разходите и ползите, докато универсалното тестване за всички хора с колоректален рак гарантира, че хората със синдром на Lynch не се пропускат. За да отговорят на разходите, изследователите се опитват да предскажат MSI или IHC директно от начина, по който туморът изглежда под микроскопа, без да правят молекулярни тестове.
Микросателитна нестабилност
Мутациите в системите за възстановяване на несъответствие на ДНК могат да доведат до затруднения в предаването на региони в ДНК, които съдържат повтарящи се модели на два или три нуклеотида (микросателити), иначе известни като микросателитна нестабилност (MSI). MSI се идентифицира чрез екстракция на ДНК както от проба от туморна тъкан, така и от нормална тъканна проба, последвана от PCR анализ на микросателитни области. MSI анализът може да се използва за идентифициране на хора, които могат да имат синдром на Lynch, и насочването им към допълнителни тестове.
Класификация
Три основни групи рак на MSI-H (микросателитна нестабилност – MSI) могат да бъдат разпознати по хистопатологични критерии:
- десни странични слабо диференцирани ракови заболявания
- десностранен муцинозен рак
- аденокарциноми на всяко място, показващи някакво измеримо ниво на интраепителни лимфоцити (TIL)
Хистопатологичните критерии не са достатъчно чувствителни, за да открият MSI от хистологията, но изследователите се опитват да използват изкуствен интелект, за да предскажат MSI от хистологията.
В допълнение, HNPCC може да бъде разделен на синдром на Lynch I (фамилен рак на дебелото черво) и синдром на Lynch II (HNPCC, свързан с други видове рак на стомашно-чревния тракт или репродуктивната система).
Предотвратяване
Скрининг тест
Генетични консултации и генетични тестове се препоръчват за семейства, които отговарят на критериите от Амстердам, за предпочитане преди появата на рак на дебелото черво.
Рак на дебелото черво
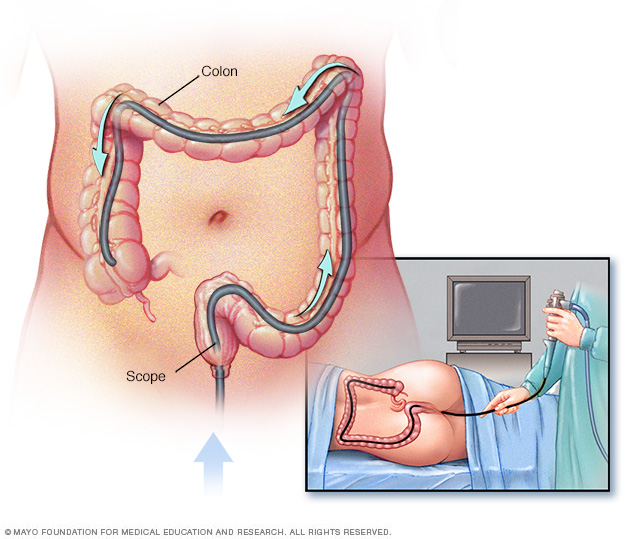
Колоноскопиите се препоръчват като превантивен метод за наблюдение на лица, които имат синдром на Lynch или гени, свързани с LS. По-конкретно се препоръчва колоноскопиите да започват на възраст 20-25 за носители на мутация MLH1 и MSH2 и 35 години за носители на мутация MSH6 и PMS2. След това колоноскопско наблюдение трябва да се извършва на 1-2 годишен интервал за пациенти със синдром на Lynch.
Рак на ендометриума / яйчниците
Ежегодно се препоръчва трансвагинален ултразвук със или без ендометриална биопсия за скрининг на рак на яйчниците и ендометриума. За жени със синдром на Lynch може да се използва годишен кръвен тест CA-125 за скрининг на рак на яйчниците, но има ограничени данни за ефикасността на този тест за намаляване на смъртността.
Други видове рак
Съществуват и стратегии за ранно откриване на други видове рак или намаляване на шансовете за тяхното развитие, които хората със синдром на Lynch могат да обсъдят със своя лекар, но ефективността им не е ясна. Тези опции включват:
- Горни ендоскопии за откриване на рак на стомаха и тънките черва на всеки 3-5 години, започвайки най-рано на 30-годишна възраст (за предпочитане в изследователска обстановка)
- Годишен анализ на урината за откриване на рак на пикочния мехур, започвайки най-рано на 30-годишна възраст (за предпочитане в изследователска обстановка)
- Годишни физически и неврологични прегледи за откриване на рак в централната нервна система (мозък или гръбначен мозък), като се започне най-рано на 25-годишна възраст
Критерии от Амстердам
Следват критериите от Амстердам при идентифициране на високорискови кандидати за молекулярно генетично тестване:
Критерии за Амстердам I (трябва да бъдат изпълнени всички точки):
- Трима или повече членове на семейството с потвърдена диагноза колоректален рак, единият от които е роднина от първа степен (родител, дете, брат или сестра) на другите двама
- Две последователни засегнати поколения
- Един или повече рака на дебелото черво, диагностицирани на възраст под 50 години
- Семейната аденоматозна полипоза (FAP) е изключена
Критериите Amsterdam II са разработени през 1999 г. и подобряват диагностичната чувствителност за синдром на Линч чрез включване на рак на ендометриума, тънките черва, уретера и бъбречното легенче.
Критерии за Амстердам II (трябва да бъдат изпълнени всички точки):
- Трима или повече членове на семейството с рак, свързан с HNPCC, единият от които е роднина от първа степен на другите двама
- Две последователни засегнати поколения
- Един или повече от свързаните с HNPCC ракови заболявания, диагностицирани на възраст под 50 години
- Семейната аденоматозна полипоза (FAP) е изключена
Хирургия
Профилактична хистеректомия и салпингооофоректомия (отстраняване на матката, фалопиевите тръби и яйчниците, за да се предотврати развитието на рак) може да се извърши преди да се развие рак на яйчниците или ендометриума.
Лечение на синдром на Lynch
Хирургията остава основната терапия за HNPCC. Пациенти със синдром на Lynch, които развиват колоректален рак, могат да бъдат лекувани или с частична колектомия, или с тотална колектомия с илеоректална анастомоза. Поради повишения риск от колоректален рак след частична колектомия и подобно качество на живот след двете операции, тоталната колектомия може да бъде предпочитано лечение за HNPCC, особено при по-млади пациенти.
Продължава противоречието относно ползата от адювантните терапии, базирани на 5-флуороурацил, за колоректални тумори, свързани с HNPCC, особено тези в стадии I и II.
- Терапията с анти-PD-1 антитела може да бъде ефективна.
Блокирането на контролни точки с терапия с анти-PD-1 сега е предпочитана терапия от първа линия за напреднала микросателитна нестабилност – високо колоректален рак.
.

















Discussion about this post